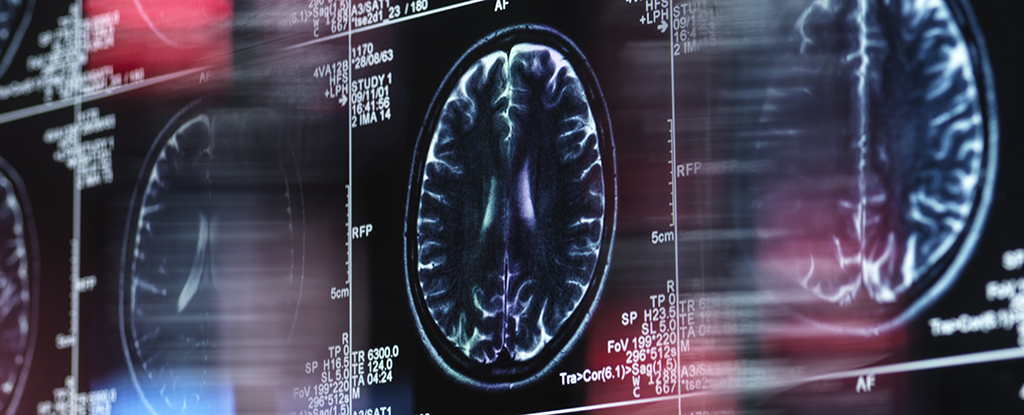
Виявлено токсичні молекули РНК, які призводять до загибелі нейронів при хворобі Альцгеймера
Токсичні ділянки РНК, які, як відомо, спричиняють самознищення клітин, були виявлені як у мозку при хворобі Альцгеймера, так і при старінні, що дозволяє запропонувати новий підхід до лікування нейродегенеративних захворювань, таких як деменція.
У дослідженні на мишах і людському мозку під керівництвом Північно-Західного університету в США вчені виявили короткі ділянки РНК (рибонуклеїнової кислоти), пов’язані з пошкодженням ДНК і загибеллю клітин у зв’язку з хворобою та супутніми факторами.
Вони також виявили, що захисні короткі ланцюжки РНК у мозку зменшуються з віком, що може сприяти прогресуванню хвороби Альцгеймера, і що люди старше 80 років з чудовою пам’яттю – так звані “суперагенти” – мають вищий рівень захисних коротких РНК.
“Ми виявили, що в старіючих клітинах мозку баланс між токсичними і захисними короткими РНК зміщується в бік токсичних”, – говорить старший автор дослідження, біохімік Маркус Пітер з Північно-Західного університету.
Приблизно кожен дев’ятий дорослий житель США старше 65 років страждає на хворобу Альцгеймера, яка характеризується розвитком амілоїд-бета бляшок, тау-сплетінь і загибеллю клітин головного мозку. Ланцюжок подій, які призводять до надмірної загибелі та порушення регуляції клітин мозку, було складно ідентифікувати.
Хоча існують ліки, які можуть сповільнити розвиток хвороби Альцгеймера, пошук більш ефективних варіантів продовжується. Автори дослідження вважають, що таргетування ланцюгів РНК відкриє нові шляхи лікування.
“Переважна частина інвестицій у розробку ліків від хвороби Альцгеймера була зосереджена на двох механізмах, – пояснює Пітер, – зменшення навантаження амілоїдними бляшками в мозку – що є відмінною рисою діагнозу хвороби Альцгеймера і становить від 70 до 80 відсотків усіх зусиль – і запобігання тау-фосфорилюванню або утворенню клубків”.
Пітер та його колеги досліджували поведінку РНК різними методами, включаючи мишачі моделі хвороби Альцгеймера, мозок мишей, мозок “людей похилого віку”, нейрони, виділені зі стовбурових клітин здорових людей та пацієнтів з хворобою Альцгеймера, а також клітинні лінії, отримані з людського мозку.
РНК переносить генетичну інформацію від ДНК до частин наших клітин, які можуть перекладати генетичний рецепт і виробляти білки, необхідні для різних клітинних функцій. Некодуючі короткі РНК відіграють певну роль у регуляції експресії генів, контролюючи білки, що кодуються довгими ланцюгами РНК, за допомогою механізму, який називається РНК-інтерференція.
Проте з віком захисні властивості РНК можуть погіршуватися і навіть ставати шкідливими.
Команда дослідників виявила, що короткі молекули РНК зі специфічними характеристиками можуть спричиняти загибель клітин. Ці токсичні короткі РНК можуть перешкоджати виробленню необхідних білків, що призводить до смерті, спричиненої елімінацією генів виживання (DISE), процесу, який активно відбувається у людей та гризунів і відіграє ключову роль у знищенні ракових клітин.
Пацієнти з хворобою Альцгеймера мають нижчі показники захворюваності на рак, що, на думку дослідників, може означати, що надмірно активний механізм DISE також сприяє загибелі клітин при хворобі Альцгеймера.
Вони виявили кореляцію між DISE, пошкодженням ДНК і загибеллю нейронів при хворобі Альцгеймера та старінням. Нейрони в мишачих моделях хвороби Альцгеймера та клітини, отримані від пацієнтів з хворобою Альцгеймера, мали знижений рівень специфічних захисних молекул короткої РНК.
Мозок, що старіє, також має менше захисних молекул РНК, що дозволяє більш токсичним коротким РНК вторгатися і здійснювати РНК-інтерференцію, в той час як у людей похилого віку їх рівень вищий.
Експерименти на клітинах, що зазнали впливу фрагментів амілоїду бета в лабораторії, показали, що загибель клітин і пошкодження ДНК збільшилися, що пов’язано з токсичними змінами РНК.
Збільшення кількості захисних РНК і підвищення активності відповідального білка, схоже, певною мірою захищає клітини, що зазнали впливу амілоїду бета, і повністю запобігає пошкодженню ДНК, яке також спостерігається у пацієнтів з хворобою Альцгеймера.
Виходячи з цих висновків, підвищення рівня захисних РНК у мозку може стати новою стратегією лікування нейродегенерації.
“Наші дані дають нове пояснення того, чому майже при всіх нейродегенеративних захворюваннях люди живуть десятиліттями без симптомів, а потім хвороба починає поступово прогресувати, оскільки клітини з віком втрачають свій захист”, – говорить Пітер.
“Стабілізація або збільшення кількості захисних коротких РНК в мозку може стати абсолютно новим підходом до зупинки або уповільнення розвитку хвороби Альцгеймера або нейродегенерації в цілому”.